סרקומה של יובינג
כל המידע שנמסר כאן הוא בעל אופי כללי בלבד, טיפול בגידולים שייכים תמיד בידי אונקולוג מנוסה!
מילים נרדפות
סרקומה של עצם, PNET (גידול עצבי-מוחי פרימיטיבי), גידול אסקין, יואינג - סרקומה בעצמות.
אנגלית: סרקומה של יואינג
הַגדָרָה
באילו סרקומה של יובינג זה מ מח עצם יוֹצֵא גידול בעצםשיכולים להופיע בין הגילאים 10-30. עם זאת, הדבר משפיע בעיקר על ילדים וצעירים עד גיל 15. הסרקומה של יואינג פחות נפוצה מזו אוסטאוסקרומה.
הסרקומה של יואינג ממוקמת באורכים עצמות ארוכות (עֶצֶם הַיָרֵך (עצם הירך) ו- שׁוּקָה (שוקה)), כמו גם באגן או בצלעות. אולם באופן עקרוני כל עצמות תא המטען ושלד הגפיים יכולות להיות מושפעות, גרורות במיוחד באזור ריאות זה אפשרי.
תדירות
ההסתברות לפתח סרקומות של יואינג היא <1: 1,000,000. מחקרים הראו כי עבור כל מיליון אנשים שגרים בה, כ- 0.6 חולים חדשים מפתחים סרקומות של יואינג מדי שנה.
בהשוואה לאוסטאוסרקומה (כ- 11%) וכונדרוסקומה (כ- 6%), הסרקומה של יואינג נמצאת במקום השלישי כמייצג נוסף של גידולי עצם ממאירים ראשוניים. בעוד שהסרקומה של יואינג מתרחשת בעיקר בין הגילאים 10-30, ניתן היה להיווצר ביטוי מרכזי בעשור השני לחיים (גיל 15). לכן זה מתבטא בעיקר בשלד ההולך וגדל, כאשר בנים (56%) סובלים מסרקומה של יואינג במקרים רבים יותר מאשר בנות. אם משווים בין גידולי העצם הממאירים הראשוניים של ילדים ומתבגרים, סרקומה של יואינג נמצאת במקום השני: בסרקומות עצמות בילדות, שיעורן של מה שמכונה אוסטאוסרקומות הוא כ- 60%, חלקן של סרקומות Ewing סביב 25%. .
סיבות
כפי שכבר הוסבר והוצג במסגרת הסיכום, הגורם שאחראי לפיתוח ה סרקומה של יובינג לא ניתן להבהיר במלואו. עם זאת נמצא כי סרקומות של יואינג מתרחשות לעיתים קרובות כאשר יש הפרעות שלד משפחתיות או חולים מתחת לאחד מלידה רטינובלסטומה (= גידול ממאיר רשתית המתרחש בגיל ההתבגרות). מחקרים הראו כי לתאי הגידול במשפחה כביכול של סרקומות יואינג יש שינוי כרומוזום מס '22 לְהַצִיג. ההערכה היא כי מוטציה זו קיימת בסביבות 95% מכלל החולים.
לוקליזציה
המיקומים הנפוצים ביותר של סרקומה של יואינג ניתן למצוא בעצמות צינוריות ארוכות, בעיקר בשוקה ובפיבולה, או בעצמות שטוחות. עם זאת, כסרטן עצם ממאיר, סרקומה של יואינג יכולה להשפיע על כל העצמות. העצמות הגדולות יותר נפגעות לרוב, הקטנות יותר לעיתים נדירות. אם העצמות הצינורות הארוכות מושפעות, הגידול נמצא בדרך כלל באזור מה שנקרא דיאפיזה, אזור הפיר.
מיקומים מועדפים:
- משוער.30% עצם הירך (עצם הירך)
- כ- 12% טיביה (שוקה)
- כ- 10% humerus (עצם הזרוע העליונה)
- אגן של כ 9%
- כ- 8% פיבולה (fibula).
בגלל הגרורות הממטוגניות הקשות המתרחשות בשלב מוקדם (ראו פרק הבא), ניתן להעלות על הדעת גם לוקליזציה ברקמות הרכות.
לוקליזציה באגן
הסרקומה של יואינג ממוקמת בעצם האגן כגידול הראשוני (אתר מוצא הגידול) כמעט בכל מקרה חמישי. אולם לעיתים קרובות יותר, הגידול הראשוני נמצא בעצם צינורית ארוכה.
הסימפטומים הראשונים יכולים להיות נפיחות, כאבים וחימום יתר באזור האגן.
לוקליזציה בכף הרגל
כף הרגל היא מקום נדיר בגידול ראשוני. מקובל יותר כי גידולים ראשוניים מהשוקה או הפיבולה מעדיפים גרורה בכף הרגל.
אם יש נפיחות כואבת וחממה יתר של כף הרגל, במיוחד בגיל ההתבגרות, יש לשלול את הסרקומה של יואינג בנוסף לדלקת מפרקים צעירה. הגרוע ביותר לא בהכרח צריך להניח כאן. אבחון ממוקד בצורה של הדמיה יכול לספק בהירות ראשונית לגבי הגורמים לתלונות.
גרורות
כאמור, זה חל סרקומה של יואינג כהורדת גרורות המטולוגיות (= דרך זרם הדם). לכן גרורות יכולות להתיישב ברקמות הרכות. מבין אלה, בעיקר הוא ריאה מושפע. עם זאת, השלד יכול להיות מושפע גם מגרורות דרך מחזור הדם.
העובדה כי יש לסווג את סרקומה של יואינג כגרורת מוקדמת מוצג על ידי מחקרים המראים כי ניתן לאתר גרורות בכ- 25% מכל המקרים בזמן האבחון. מכיוון שלצערנו לא תמיד ניתן לגלות גרורות, ככל הנראה קצב האפל יהיה גבוה בהרבה.
אִבחוּן
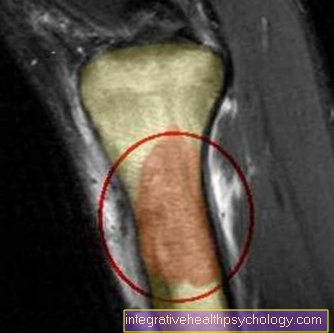
סרקומות יובלות עלולות לגרום לתופעות מגוונות. הם צריכים להיות רשומים להלן:
- כאב מסיבה לא ידועה
- נפיחות ובדרך כלל כאבים באזור / ה המושפעים / ים
- נפיחות בבלוטות הלימפה
- סימנים מקומיים לדלקת (אדמומיות, נפיחות, התחממות יתר)
- ירידה לא רצויה במשקל
- הגבלות תפקודיות עד שיתוק
- שבר ללא אירוע תאונה
- זיעת לילה
- לויקוציטוזיס בינוני (= עלייה במספר הלוקוציטים בדם)
- ירידה בביצועים
ניתן לשלול גידול עם הסתברות מספקת אם מתקיימים הקריטריונים הבאים בהתאם לאבחון קליני, הדמיה ומעבדה:
- אין שום עדות למיסה
אוֹ
ניתן להסביר ולתעד את הנפיחות הנראית לעין, המוני המוכח או תלונות לא ברורות על ידי מחלה שאינה גידולית.
אבחון בסיסי:
באופן עקרוני, שיטות הדמיה משמשות לאבחון בסיסי. אלו הם
בדיקת רנטגן
בדיקת רנטגן באזור לוקליזציה של הגידול (לפחות 2 רמות)
סונוגרפיה
סונוגרפיה של הגידול (במיוחד אם יש חשד לגידול ברקמות רכות באבחון המבדל)
על מנת לקבל מידע נוסף וכדי לאפשר תיחום אבחנות דיפרנציאלי, נעשה שימוש באבחון מעבדה (בחינת ערכי המעבדה). הערכים הבאים נקבעים כחלק מאבחון מעבדה זה:
- ספירת דם
- ברזל (בגלל ירידה בגידולים)
- אלקטרוליטים (כדי לשלול היפר קלצמיה)
- ESR (שיעור משקעים)
- CRP (חלבון תגובתי C)
- פוספטז אלקליין (AP)
- עצם ספציפית (AP)
- חומצה פוספטז (sP)
- אנטיגן ספציפי לערמונית (PSA)
- חומצת שתן (HRS): גדל עם תחלופת תאים גבוהה, למשל בהמובלסטוזיס
- סך החלבון: ירידה בתהליכי צריכה
אלקטרופורזה של חלבון - מצב שתן: פרפרוטאינים - עדות למיאלומה (פלסמיטומה)
- סמן גידול NSE = אנולאז ספציפי נוירוני בסרקומה של יואינג
אבחון מיוחד לגידול
הדמיית תהודה מגנטית (MRI)
בנוסף לשיטות ההדמיה המוזכרות בהקשר של אבחון בסיסי, טומוגרפיה של תהודה מגנטית מייצגת אפשרות נוספת שניתן להשתמש בה במקרים בודדים.
בעזרת MRI (טומוגרפיה של תהודה מגנטית) ניתן להראות היטב את הרקמות הרכות, לפיה ניתן להציג את התרחבות הגידול למבנים שכנים (עצבים, כלי) של העצמות הפגועות. יתר על כן, ניתן לאמוד את נפח הגידול באמצעות MRI (טומוגרפיה של תהודה מגנטית) וניתן להבהיר את היקף הגידול המקומי.
ברגע שיש חשד לגידול עצם ממאיר, יש לצלם את כל העצם נושאת הגידול כדי לא לכלול גרורות (התנחלויות ממאירות).
טומוגרפיה ממוחשבת (CT):
(במיוחד להצגת מבני עצם קשים (קליפת המוח))
טומוגרפיה לפליטת פוזיטרון (PET)
(הערך עדיין לא תקף מספיק)
קרא עוד בנושא: טומוגרפיה לפליטת פוזיטרון
אנגיוגרפיה של חיסור דיגיטלי (DSA) או אנגיוגרפיה להמחשת כלי הגידול
Scintigraphy שלדי (scintigraphy תלת פאזי)
בִּיוֹפְּסִיָה
כאמור מספר פעמים לעיל, ההבחנה בין סרקומה של יואינג לאוסטאומיאליטיס למשל יכולה להיות קשה למדי. בנוסף לעובדה שהתסמינים דומים, תמונת הרנטגן ככזו לא תמיד יכולה לספק מידע ישיר. אם לאחר האבחנה הלא-פולשנית שנקרא לעיל, עדיין קיים חשד לגידול או אם קיימת אי וודאות לגבי סוג הגידול וכבודו, יש לבצע בדיקה היסטופתולוגית (= בדיקת רקמות).
נהלים פתוחים
ביופסיה חותכת
כחלק מהביופסיה החתוכה שנקראת, הגידול נחשף באופן כירורגי בחלקו. לבסוף, נלקחת דגימת רקמות (במידת האפשר עצם ורקמות רכות). ניתן להעריך ישירות את רקמת הגידול שהוסרה.
ביופסיה מרתקת (הסרת גידול מלאה)
זה נחשב רק במקרים חריגים, למשל אם יש חשד לממאירות (שינוי מגידול שפיר לגידול ממאיר) של אוסטאוכונדרומות קטנות יותר.
תֶרַפּיָה
הגישה הטיפולית כאן היא לרוב בכמה מישורים. מצד אחד, תוכנית הטיפול המכונה בדרך כלל מספקת טיפול כימותרפי לפני הניתוח (= כימותרפיה ניאו-אדג'ובנטית). גם לאחר הסרת הניתוח של סרקומה של יואינג, ניתן טיפול מעקב טיפולי באמצעות הקרנות ובמידת הצורך חידוש כימותרפיה. כאן מורגש הבדל לאוסטאוסרקומה: בהשוואה לסרקומה של יואינג, לאוסטאוסרקומה יש רגישות לקרינה נמוכה יותר.
יעדי טיפול:
גישה טיפולית כביכול (ריפוי) ניתנת במיוחד בחולים שסרקומת יואינג היא מקומית ואינה מציגה גרורות. בינתיים, מה שמכונה כימותרפיה ניאו-אדג'ובנטית בשילוב עם ניתוח והקרנות פותחים הזדמנויות נוספות. אם גרורת סרקומה של יואינג מחוצה גרורות מחוץ לריאות (= מחלת גידול כללית; גרורות חוץ-ריאתיות), הטיפול בדרך כלל בעל אופי פליאטיבי (מאריך חיים) (ראה בהמשך).
שיטות טיפול:
מְקוֹמִי:
- כימותרפיה לפני הניתוח
- טיפול כירורגי (כריתה רחבה או רדיקלית לאחר אנקינג)
- רדיותרפיה
מערכתית:
כימותרפיה אנטי-פלסטית
- טיפול משולב (בעיקר (= "שורה ראשונה"): דוקסורוביצין, ifosfamide, מטוטרקסט / לוקובורין, ציספלטין; בשורה השנייה (= "שורה שנייה"): etoposide ו carboplatin)
(פרוטוקולים יכולים להשתנות בהתראה קצרה)
טיפול מרפא:
- כימותרפיה אגרסיבית מרובת חומרים לפני ואחרי הניתוח
- טיפול מקומי בצורה של כריתת גידולים כירורגיים או קרינה בלבד
- יש להוסיף את הטיפול באמצעות טרום הקרנה (למשל במקרה של גידולים שאינם ניתנים להפעלה, שאינם מגיבים) או באמצעות הקרנה לאחר ההקרנה
- חשוב להזכיר בהקשר של טיפול כירורגי, שלא מעט בגלל התפתחות נוספת של שיטות כירורגיות, התערבויות המשמרות את הגפיים אפשריות במקרים רבים. עם זאת, סיכויי הריפוי תמיד בעלי עדיפות עליונה, כך שהמיקוד צריך תמיד להיות ברדיקליות (= איכות אונקולוגית) ולא באובדן תפקוד אפשרי.
- לאחר מכן ניתן להמשיך בכימותרפיה (ראה לעיל). לאחר מכן אחד מדבר על מה שמכונה איחוד.
- בחולים עם גרורות ריאה יתכן שיהיה צורך בהתערבויות נוספות באזור הריאות, כגון הסרה חלקית של הריאות.
טיפול פליאטיבי (מאריך חיים):
חולים עם מחלת גידול כללית (= גרורות חוץ-ריאתיות) צריכים לאתר את הגידול הראשוני על תא המטען ו / או שהגידול הראשוני יתגלה כבלתי ניתן לפעולה. במקרים כאלה, בדרך כלל רק טיפול פליאטיבי אפשרי. במקרים כאלה המוקד הוא בדרך כלל בשמירה על איכות חיים, כך שהטיפול מתמקד בהקלה בכאב ובשמירה על התפקוד.
תַחֲזִית
האם התרחשות הישנות או לא תלויה מאוד במידת הגרורות, בתגובה לכימותרפיה לפני הניתוח ו"הטבע הרדיקלי "של הסרת הגידול. כיום מעריכים כי שיעור ההישרדות לחמש שנים הוא סביב 50%. השיפורים התפעוליים במיוחד אפשרו לשפר את ההסתברות להישרדות במהלך 25 השנים האחרונות
שיעור ההישרדות יורד עם גרורות ראשוניות. כאן שיעור ההישרדות הוא סביב 35%.
סיכויי החלמה
בדומה לסוגי סרטן אחרים, סיכויי ההחלמה מהסרקומה של יואינג נראים בתחילה כשונים באופן אינדיבידואלי, מכיוון שהסטטיסטיקה רק מראה אי פעם את שיעורי ההתאוששות וההישרדות הממוצע.
הסיכוי להחלמה מוגבר אם ניתן להסיר את הגידול באופן ניתוחי לחלוטין. לפני כן יש לעשות כימותרפיה בכדי לכווץ את הגידול. לאחר הסרת הגידול בניתוח, יש לבצע כימותרפיה נוספת בכדי להרוג את כל תאי הגידול שנותרו.
אם לא ניתן להסיר לחלוטין את הגידול בניתוח, הסיכוי להחלמה הוא הרבה יותר גרוע. טיפול מעקב בכימותרפיה צריך להתקיים גם כאן.
בהחלט צריך להקרין גידול שלא ניתן לנתח.
באופן כללי ניתן לומר כי הסיכוי לריפוי לסרקומה של יואו הוא גרוע יותר אם כבר קיימות גרורות בזמן האבחנה. המשמעות היא שהגידול התפשט וגדל גם במקומות אחרים בגוף.
שיעור הישרדות
שיעורי ההישרדות באופן כללי ניתנים ברפואה כערך הסטטיסטי של "שיעור ההישרדות ל -5 שנים". זה מצביע באחוזים עד כמה גדול מספר הניצולים לאחר 5 שנים בקבוצת מטופלים מוגדרת. שיעור ההישרדות המדווח לסרקומה של יואינג נע בין 40% ל 60-70%. אזורים רחבים אלה נובעים מהעובדה ששיעור ההישרדות תלוי בהתפשטות אזור העצם בהתאמה. לדוגמה, אם עצמות הזרועות ו / או הרגליים מושפעות, שיעור ההישרדות ל -5 שנים הוא 60-70%. אם עצמות האגן מושפעות, זה 40%.
כמה גבוה הוא הסיכון להישנות?
שיעור ההישרדות לחמש שנים ממוצע של 50%. כאן ניתן להניח שמדובר בסרטן אגרסיבי וממאיר. שיעור ההישרדות לחמש שנים אומר כי בממוצע מחצית מכל סרקומות יואינג שאובחנו מובילות למוות.
עם זאת, אם לא ניתן לאתר ממצאים נוספים לאחר 5 שנים לאחר הטיפול המוצלח בסרקומה של יואינג, נאמר כי הסרטן נרפא.
טִפּוּל עוֹקֵב
המלצות:
- בשנה 1 ו -2:
יש לבצע בדיקה קלינית אחת לשלושה חודשים. ככלל, בדיקת רנטגן מקומית, בדיקות מעבדה, בדיקת בדיקת מעבדה בֵּית הַחָזֶה ובוצע סקינטיגראפי שלד מלא. בדיקת בדיקת MRI מקומית נעשית בדרך כלל אחת לשישה חודשים. - בשנה 3 עד 5:
יש לבצע בדיקה קלינית אחת לחצי שנה. ככלל, בדיקת רנטגן מקומית, בדיקות מעבדה, בדיקת בדיקת מעבדה בֵּית הַחָזֶה ובוצע סקינטיגראפי שלד מלא. בדיקת MRI מקומית מתבצעת בדרך כלל פעם בשנה. - משנה 6 ואילך, בדרך כלל הדברים הבאים מתרחשים פעם בשנה:
בדיקת רנטגן עם בדיקת מעבדה ובדיקת CT של החזה וכן בדיקת סקרטיגרפיה שלד ושלם ו- MRI מקומי.
סיכום
המחלה (סרקומה של יואינג) קיבלה את שמה מהתיאור הראשון של ג'יימס יואינג בשנת 1921. מדובר בגידולים ממאירים מאוד הנובעים מתאי עצב פרימיטיביים פרימיטיביים (= תאי מבשר לא בשלים של תאי עצב). לפיכך, סרקומות יואינג שייכות לגידולים הפרימיטיביים, הממאירים והמוצקים.
כאמור לעיל, סרקומות של יואינג משפיעות בעיקר על האזורים האמצעיים של העצמות הצינוריות הארוכות והאגן, אולם ניתן להעלות על הדעת גם נגע לזרוע העליונה (= humerus) או לצלעות, כך שתופיע מקבילות לאוסטאוסרקומה. בשל הסימנים הנלווים לדלקת, בלבול עם אוסטאומיאליטיס אפשרי.
בשל גרורות המתרחשות מהר מאוד (כ- ¼ מכלל החולים כבר מראים כביכול התיישבות בת בזמן האבחנה), ניתן למצוא סרקומות של יואינג ברקמות רכות, בדומה ל rhabdomyosarcomas. הריאות בדרך כלל מושפעות בעיקר מגרורות.
הסיבות שיכולות להיות אחראיות להתפתחות סרקומה של יואינג אינן ידועות עדיין. עם זאת, כיום ההנחה היא כי לא המרכיב הגנטי (תורשה) או הקרנות שכבר בוצעו אינם יכולים להיות אחראים לפיתוח. עם זאת, נמצא כי סרקומות של יואינג מתרחשות לעיתים קרובות כאשר יש הפרעות שלד משפחתיות או כאשר חולים סובלים מרטינובלסטומה (= גידול רשתית ממאיר המופיע בגיל ההתבגרות) מלידה. מחקרים הראו כי תאי הגידול מהמשפחה המכונה סרקומות של יואינג מראים שינוי בכרומוזום מספר 22. ההנחה היא שמוטציה זו (שינוי גנטי) קיימת בסביבות 95% מכלל החולים.
סריקומות של יובש יכולות לגרום לנפיחות וכאבים באזור / ה המושפעים, אשר יכולים להיות קשורים גם ללקויות תפקודיות. ניתן להעלות על הדעת חום ולוקוציטוזיס בינוני (= עלייה במספר הלוקוציטים בדם). בגלל האפשרות לבלבול עם אוסטאומיאליט, למשל (ראה לעיל), אבחנה לא תמיד קלה ולכן, בנוסף לנהלי ההדמיה (בדיקת רנטגן), ייתכן שיהיה צורך לבצע ביופסיה (= בדיקת רקמות של דגימת רקמות).
הגישה הטיפולית כאן היא לרוב בכמה מישורים. מצד אחד, תוכנית הטיפול המכונה בדרך כלל מספקת טיפול כימותרפי לפני הניתוח (= כימותרפיה ניאו-אדג'ובנטית). גם לאחר הסרת הניתוח של סרקומה של יואינג, ניתן טיפול מעקב טיפולי באמצעות הקרנות ובמידת הצורך חידוש כימותרפיה. כאן מורגש הבדל לאוסטאוסרקומה: בהשוואה לסרקומה של יואינג, לאוסטאוסרקומה יש רגישות לקרינה נמוכה יותר.
האם התרחשות הישנות (צמיחת גידול מחודשת) ובין אם לא, תלויה במידה רבה במידת הגרורות, בתגובה לכימותרפיה לפני הניתוח וב"אופי הרדיקלי "של הסרת הגידול. כיום מעריכים כי שיעור ההישרדות לחמש שנים הוא סביב 50%. השיפורים התפעוליים במיוחד אפשרו לשפר את ההסתברות להישרדות במהלך 25 השנים האחרונות