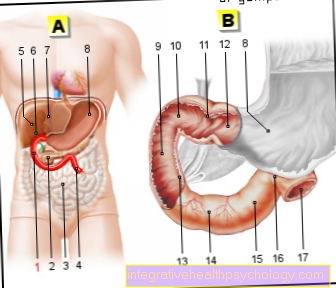
חשיבות הביופסיה לאבחון סרטן השד
מילים נרדפות במובן הרחב יותר
ביופסיה, שאיפת מחט עדינה, ביופסיית אגרוף, ביופסיה ואקום, MIBB = ביופסיה של חזה פולשני באופן מינימלי, ביופסיה חריגה.

ביופסיה (דגימת רקמות)
לעתים קרובות, למרות מיצוי כל אפשרויות האבחון, רק ביופסיה מספקת סוף סוף בהירות בשאלה האם זו אחת שָׁפִיר או אחד גידול ממאיר מעשים. אז אם בביופסיה נעשית, זה לא בהכרח אומר שיש לך סרטן. ניתן היום לראות כמעט את כל הממצאים הלא תקינים או החשודים שנמצאו ב חזה לביופסיה, כלומר קח מדגם וקבע אבחנה. קל לבצע ביופסיה, כמעט ולא מכביד על רקמת השד ובדרך כלל ניתן לבצע אותה ללא אשפוז, אך הבדיקה יכולה להיות כואבת. לאחר מכן נלקח הדגימה על ידי פתולוג - א מומחים במחקרי רקמות ותאים - בדק. הפתולוג יכול להשתמש בתאים ברקמה כדי לאבחן, מאחר ותאי סרטן נראים שונים מתאים בריאים. אחד מדבר על רקמה או בדיקה היסטולוגית.
קרא עוד על נושא זה כאן: בִּיוֹפְּסִיָה
בעבר היה צורך לבצע חתך להסרת חתיכת רקמה. מה שמכונה כיום נהלים זעירים פולשניים, בהם נלקחות דגימות עם מחטים על מנת להגן על רקמת השד ככל האפשר.
ישנן שיטות רבות לעשות זאת, ממחטים דקות במיוחד ועד מחטים חלולות עבות יחסית. המחשבה להיתקע בחזה עם מחט מפחידה לרוב הנשים. החלק הכי לא נוח בבדיקה הוא הרגע בו נקב העור, תלוי בקוטר הקנולה בה נעשה שימוש, תרגישו פחות או יותר כאב, בדומה לנטילת דגימת דם. העור מורדם תחילה באופן מקומי. עם זאת, בקושי ניתן להרגיש את התנועה של המחט ברקמת השד.
אפשרות הביופסיה יכולה למנוע ניתוחים מיותרים רבים (ראו גם ניתוח סרטן שד). בעיקרון ניתן לחלק את השיטות השונות לשתי קטגוריות. במקרה של ממצאים מוחשיים, ניקוב מחט דק וביופסיית אגרוף מונחה אולטראסאונד הן שיטות אפשריות. במקרה של ממצאים הניתנים לגילוי רק על ידי ממוגרפיה, קיימים פעולות ביופסיה סטראוטקטיות (ראה להלן).
אם הממצאים מוכרים כ שפירים לאחר שנלקחה דגימת הרקמה, אין צורך בהתערבות נוספת. ההליך הנוסף תלוי בתלונות המטופל. ניתן להסיר את הגוש אם הוא גורם לכאב, ממשיך לצמוח או שהוא פשוט טורד ו / או מטריד.
אולם בהתאם לגודל הגוש, הדבר עלול לגרום לנסיגות, שינויים בצורתם וצלקות על השד, מה שבתורו יכול להוביל לכאבים.
קרא עוד בנושא בכתובת: ביופסיה של השד
מה יכול הפתולוג לזהות מדגימה של רקמות?
בהתבסס על דגימת הרקמות, הפתולוג יכול לספק תחילה מידע אם השינוי הוא שפיר או ממאיר. א חיובי יותר ממצא פירושו בהקשר זה כי הממצא חיובי לסרטן, כלומר ממאיר. ההפך הוא עם אחת שלילי לא נמצא שום עדות לסרטן. גם בבדיקות אחרות "חיובי" פירושו תמיד בשפת הפתולוגים שמשהו התגלה או קיים, ולא שזו תוצאה "טובה" עבור המטופל.
הפתולוג יכול גם לקבוע את מקור התאים. משמעות הדבר היא שהוא יכול לדעת בדרך כלל אם גוש בכבד הוא סרטן הכבד או האם, למשל, גידול הבת של סרטן השד קיים. הפתולוג משתמש במדגם הרקמות כדי ליצור מעין "פרופיל גידול", כלומר רשימה של מאפייני הגידול. הרופאים המטפלים יכולים להשתמש בזה כבסיס לגישתם הטיפולית ולהצהיר על הפרוגנוזה של סרטן השד.
אם יש שינויים בתאים, הפתולוג יוצר "דירוג". דירוג התאים מעיד עד כמה התאים עדיין דומים לרקמתם המקורית, או להפך, עד כמה הם השתנו. זה נקרא גם מידת ההתמיינות של התאים. בנוסף, שינויים אופייניים בגרעיני התא וההתרחשות של נמק (רקמה מתה) כיבדו. "דירוג" התאים משפיע על הפרוגנוזה ועל אסטרטגיות הטיפול האפשריות ומעיד על התוקפנות של הגידול.
אנא קרא גם את העמוד שלנו שלבי סרטן השד
באמצעות שיטות בדיקה שונות, הפתולוג יכול גם להצהיר על תכונות אחרות של התאים שהופכות אותם לרגישים במיוחד לצורות מסוימות של טיפול ובאותה עת יש השפעה על הפרוגנוזה. זה כולל קולטנים מסוימים שיש לתאי הגידול ולחלקם אין.
אנא קרא גם את העמוד שלנו סמני גידול בסרטן השד
מידע: דרגת בידול
ככל שהדירוג גבוה יותר, כך תאי הגידול דומים לתאים בריאים וסרטן אגרסיבי יותר.
יש שלוש דרגות:
• G1 פירושו "מובחן היטב",
• G2 פירושו "בידול בינוני",
• G3 פירושו "בידול גרוע".
כ- 60 מתוך 100 גידולים מסווגים כ- G2.
בחינת דגימת הרקמה
בדיקה ביוכימית מתבצעת על דגימת הרקמות כדי לקבוע את הרגישות והכמות של קולטני ההורמונים על תאי הסרטן. ח. כמות הקולטנים להורמוני המין הנשיים אסטרוגן ופרוגסטרון. מכיוון שתאי הגידול מאופיינים בכך שהתפקודים התקינים של תא מופרעים, זה יכול להוביל גם לאובדן היכולת לייצר קולטנים להורמוני המין. מבדילים בין תאי סרטן שד חיובי לקולטני אסטרוגן (סוגים של סרטן שד). הבחנה זו ממלאת תפקיד מעל הכל מבחינת אפשרויות הטיפול. אם ישנם קולטנים רבים, זהו סימן לכך שהסרטן מגיב היטב לטיפול הורמונלי.
בדיקה נוספת של דגימת הרקמות תקבע אם תאי הגידול מכילים קולטני HER2 / neu רבים. באמצעות קולטנים אלה גורמי צמיחה יכולים "לעגון" לתא סרטן השד ולעורר אותו להתחלק יותר ולגידול לצמוח מהר יותר. ניתן למנוע עגינה זו באמצעות טיפול בנוגדנים.
קרא עוד בנושא: איך אתה מזהה סרטן שד?
מה הסיכונים של ביופסיה?
עם כולם בִּיוֹפְּסִיָה קיים סיכון קטן לזיהום ו / או לדימום. יכול דרך ערוץ הניקוב בַּקטֶרִיָה חודרים לרקמת השד וגורמים לדלקת שם, אך זה נדיר ביותר. דרך הניקוב בחזה כלי דם להיפצע, וזה בתורו מוביל לקטנים יותר מְדַמֵם יכול להוביל. הסכנה היחידה כאן היא אם המטופל למשל יש הפרעת קרישת דם או תרופות נוגדות קרישה כובש (למשל אַספִּירִין). בכדי להבהיר זאת מראש, נלקח דם לפני כל ביופסיה ונבדק קרישת הדם, וכן רשימה של אלו שנלקחו תרופות נוצר.
קרא עוד על הנושא כאן: בִּיוֹפְּסִיָה
כמה זמן לוקח הדגימה?
כמה זמן לוקח דגימת רקמות בכל מקרה פרטני תלוי הן בסוג הביופסיה והן ברופא המבצע את הבדיקה. זה נעשה בעיקר במסגרת חוץ אשפוזית, מה שאומר שמטופלים יכולים בדרך כלל לחזור הביתה לאחר החזרה. בדרך כלל ההסרה נמשכת מספר דקות ונבדקת בטכניקות הדמיה. ניקוב המחט כמעט ולא מורגש, מכיוון שהעור והרקמה באזור הניקוב הופכים באופן זמני לבלתי רגישים לכאבים עם הרדמה מקומית. לאחר האיסוף מוצבים תחבושת לחץ על שטח דגימת הרקמה. כדי למנוע סיבוכים חריפים, על המטופלים להישאר תחת טיפול רפואי מספר שעות לצורך התבוננות על מנת לשלול דימום משני, אך הם יכולים לחזור לביתם באותו יום.
מה יש לקחת בחשבון לאחר ההסרה?
הביופסיה לסיווג ממצא שפיר או ממאיר בשד היא הליך המתבצע לעתים קרובות ולעיתים נדירות מוביל לסיבוכים. דימום קל וכך נוצרת חבורה באזור דגימת הרקמה תקינה ונעלמת לאחר מספר ימים. בהתאם לשיטת האיסוף, יכולה להיווצר צלקת קטנה. סיבוך של זה יכול להיות היווצרות גידול צלקת, שלרוב הופכת רק לבעיה קוסמטית. עם זאת, אם השד ממשיך לדמם בכבדות ובעקשנות בימים שלאחר ההליך, יתכן שזו תוצאה לא רצויה של הביופסיה ויש להציג אותה לרופא באופן מיידי. בכדי להימנע מתוצאה זו, בדרך כלל מומלץ ללבוש תחבושת לחץ חזקה ומתאימה ולדאוג לעצמך לאחר נטילת הדגימה. במקרים נדירים, ההליך יכול גם להכניס חיידקים לאזור הנקב, שעלול לגרום לדלקת. לכן חשוב לא ללכת לבריכות או לסאונות בשעות או בימים שלאחר הצילום של הדגימה. אם אתר הניקוב הופך לאדום, נפוח, מחומם יתר על המידה או הופך לרגיש יותר ללחץ, יש לפנות לרופא המטפל כדי לשלול דלקת, או במידת הצורך לטפל בה בזמן.
האם תאי סרטן מועברים במהלך ביופסיה?
מכיוון ששאלה זו נשאלת לעיתים קרובות, יש לשים לב לסיכון זה במיוחד. מטופלים חוששים כי נטילת דגימת רקמות עלולה להפיץ תאי סרטן לשד. חשש זה אינו מבוסס. מחקרים הראו זאת גידול של תאים סרטניים בודדים ברקמה הנקובה אינו סביר ביותר. עם זאת ישנם הבדלים בין צורות סרטן שונות ובין טכניקות האיסוף השונות. עבור שני סוגי הסרטן איפה ביופסיות מבוצעים בתדירות גבוהה ביותר באבחון, סרטן השד ו סרטן הערמונית עד כה אין שום עדות לכך שתאי הגידול שהועברו הובילו להתפתחות מוקדי סרטן חדשים. עם זאת, בסוגים אחרים של סרטן זה יכול להיות שכיח יותר, למשל. עם סוגים מסוימים של סרטן שחלות. לעולם לא ניתן לשלול את הסיכון לחלוטין.
איזה צורת ביופסיה משמש בסוף ניתן לבירור רק בדיון פרטני עם הרופא המטפל. המידע הבא מייצג אפוא רק מידע רקע כללי: תמיד יש שינויים חדשים בטכניקות הדגימה שתוארו, השונים זה מזה בפרטים ואנחנו מנסים כל הזמן לשפר את הטכניקות הנוכחיות.
ניקוב מחט עדין
בתוך ה ניקוב מחט עדין תאים בודדים או אשכולות תאים נלקחים ישירות מהצומת בעזרת מזרק וקנולה דקה מאוד (בקוטר 0.5 מ"מ בלבד, שהיא דקה יותר מסיכה). תוצאות הבדיקה זמינות בדרך כלל באותו יום. איכות ניקוב המחט הדק תלויה רבות בניסיון של הבודק. במקרה של ממצאים ממאירים, האבחון בטוח ב -96%. עם ממצאים שפירים לרוע המזל רק 90%, כלומר עם גוש מוחשי, לא תמיד תוכלו לסמוך על תוצאה שלילית. מכיוון שרק תאים בודדים מוסרים במהלך שאיפת מחט דקה ולא חתיכות רקמות שלמות, זה יכול להיות קשה לפתולוג להצהיר, למשל. לגבי דירוג או סוג גידול שיש לבצע. במידת הצורך, א אגרוף ביופסיה לְהֵעָשׂוֹת. ניקוב המחט העדין משמש רק כמה בודקים המתמחים ומוחלף יותר ויותר על ידי הביופסיה של האגרוף.
אגרוף ביופסיה
הביופסיה של האגרוף היא דרך נוספת לקחת דגימת רקמות מממצא מישוש ו / או ממוגרפיה לא תקינים. לרקמה נורה מחט בקוטר של כ- 1.6 מ"מ במהירות גבוהה. טכניקה זו מבטיחה כי החדרת המחט אינה נוחה יותר מנטילת דם. עם זאת, יש צורך גם בחתך עור קטן בהרדמה מקומית. בוחן מנוסה יורה את המחט ישירות לממצאים המדוברים "מתחת לטווח הראייה". פירושו של ראייה פירושו שבדיקת אולטרסאונד של השד מתבצעת בו זמנית, עליה ניתן לראות את הממצאים, המחט ומיקומה. בדרך כלל נלקחים שלושה אגרופים שונים משלושה אזורים שונים בגידול, אך יתכן ויהיה צורך גם באגרופים נוספים.
ביופסיה של אגרוף יכולה להסיר יותר רקמות מאשר שאיפת מחט עדינה. בתוך המחט יש חלל בו ניתן לקבל תחבושת רקמה כנקוב. לאחר מכן נשלח הדגימה לפתולוג. עם ביופסיה של אגרוף, האבחנה כמעט ודאית כמו הסרה כירורגית של הגידול: במקרה של ממצא ממאיר, וודאות האבחנה היא 98%, ובמקרה של ממצאים שפירים הוודאות היא מעל 90%. ביופסיית האגרוף יכולה להימנע מהתערבויות כירורגיות רבות ומיותר במקרה של ממצאים שפירים.
נהלים סטראוטקטיים
המונחים סטראוטקטיים (סטריאו = מרחביים, מוניות = סדר או כיוון) מסכמים טכניקות שונות בהן העבודה מתבצעת תחת בקרת רנטגן. על ידי צילום מספר תמונות מכיוונים שונים, הרופא יכול להתמצא במרחב תוך ביצוע הביופסיה ולאתר את הממצאים במדויק.
נהלים סטראוטקטיים משמשים לרוב לביופסיה של ממצאים המשמשים רק ב ממוגרפיה ניתן לראות, למשל בולט הסתיידות מיקרו בחזה. ההבדל היחיד בין הטכניקות השונות הוא המחט המשמשת וכמות דגימות הרקמות שנלקחות. הממוגרפיה הדיגיטלית משמשת כיום בעיקר כבקרת רנטגן. בניגוד לממוגרפיה המקובלת, התמונות זמינות מיידית ומשך הבדיקה מצטמצם מאוד.
ביופסיה סטראוטקטית ושאיפת מחט עדינה
שני הנהלים פועלים בדיוק כפי שתואר לעיל, עם ההבדל שה- קולי כאן דרך אחד מכונת ממוגרפיה מוחלף. נטילת הביופסיה מעט יותר לא נוחה מכיוון שהמטופל נאלץ לשבת בשקט זמן רב בזמן שהשד דחוס במכשיר הממוגרפיה לצורך ההקלטה. בנוסף, קיימת חשיפת הקרינה מהקלטות מרובות, הנחוצות כדי לאתר את הממצאים במרחב תלת ממדי. אפילו עם ביופסיה סטראוטיפטית של ניקוב / ניקוב מחט דק, האמינות של התוצאות גבוהה מאוד אם מתגלה הממצא. עם זאת, רק במרפאות מעטות יש את היכולות הטכניות עבור אחת ביופסיה אגרופה סטראוטיפטית.
ביופסיה ואקום (MIBB = ביופסיה של שד זעיר פולשנית)
ביופסיית הוואקום (MIBB = ביופסיה של חזה זעיר פולשנית) הוא פיתוח נוסף של ביופסיות מחט פולשניות מינימליות פולשניות. שם נוסף לשיטה זו הוא ביופסיה ואקום של mammotome. הוא משמש כאשר ממוגרפיה מוצאת רקמות משתנות בגודל חמישה מילימטרים או יותר. ניתן לשלב את ביופסיית הוואקום בשתי שיטות הדמיה, ממוגרפיה ואולטרה סאונד. השילוב עם ממוגרפיה נפוץ יותר, וזו הסיבה שהוא נחשב בין הנהלים הסטראוטקטיים.
רוב הזמן, המטופלת שוכבת על בטנה על שולחן בדיקה מיוחד עם פתח בו השד מונח כך שהוא לא יכול להזיז או להחליק במהלך הבדיקה. מחט חלולה בעובי של שלושה מילימטרים משמשת לביופסיית הוואקום. לאחר הרדמה מקומית מוחדרת המחט החלולה לשד דרך חתך באורך 3-4 מ"מ. על ידי לחץ שלילי (לִשְׁאוֹב) רקמה נשאבת למחט החלולה, בה יש סכין זעירה במהירות גבוהה המפרידה בין המצוץ במדגם לשאר הרקמה. לאחר מכן מועברים את הרקמה אל פתח באמצע המחט, וממנה ניתן להסיר אותה באמצעות פינצטה. המחט יכולה להסתובב סביב ציר משלה כאשר מוסרים את הרקמה כך שניתן לקחת דגימות מכמה נקודות של הממצאים והסביבה. זה מגביר את אמינות האבחנה. בחלק מהמרפאות יש מכשירים מיוחדים שבהם ניתן לבצע את ביופסיית הוואקום גם בישיבה. בנוסף, בעזרת טכניקה זו ניתן להכניס מיקרו קליפ לאחר שנלקחו הדגימות, המסמן את מיקום אוסף הדגימות לבדיקות או פעולות בקרה מאוחרות יותר.
ביופסיה מרתקת
א ביופסיה מרתקת הוא הליך כירורגי; לכן זה נקרא גם ביופסיה אופרטיבית או פתוחה. בתוך הרדמה כללית כל האזור החשוד מוסר מהאזור חזה הוסר ואז נלקח לבדיקה על ידי הפתולוג. האישור הסופי לאבחון יכול להיעשות רק על ידי הסרת גוש השד לאחר מכן בדיקת רקמות מיקרוסקופיות בהתאמה. לפיכך, ביופסיה חריגה היא עדיין ההליך הסטנדרטי במרכזים רבים. אבל זה גם הנוהל עם הכי הרבה תופעות לוואי.
עבור נשים רבות הצלקת שאורכה 3-4 ס"מ שנותרה על השד מעצבנת מאוד. נזק לרקמות יכול גם להוביל לנסיגות והידבקויות בתוך השד. זה מקשה לשפוט את הדברים בהמשך ממוגרפיה. מכיוון שרוב הביופסיות שבוצעו מביאות לתוצאות שליליות, חלק מהרופאים שואלים את עצמם האם התועלת עבור נשים עם תוצאה חיובית בהשוואה להליכים פחות פולשניים אחרים באמת עולה על הנזק שנשים עם תוצאה שלילית.
קרא עוד על נושא זה כאן: בִּיוֹפְּסִיָה