מחלות גנטיות
הַגדָרָה
מחלה גנטית או מחלה תורשתית היא מחלה הנגרמת על ידי אחד הגנים או יותר של האדם הנוגע בדבר. ה- DNA פועל כאן כטריגר ישיר של המחלה. ברוב המחלות הגנטיות ידועים מיקומי הגנים הסיבתיים. אם יש חשד למחלה גנטית, ניתן אפוא לבצע את האבחנה בהתאמה באמצעות בדיקה גנטית.
מצד שני, יש גם מספר רב של מחלות שההופעה שלהן משפיעה גנטית או עליהן נדון, כמו סוכרת ("סוכרת"), אוסטאופורוזיס או דיכאון. מדובר בנטיות שנקראות, כלומר הסבירות מוגברת למחלות מסוימות. יש להבחין בנטיות בין מחלות תורשתיות.

מדובר במחלות תורשתיות נפוצות
באופן מוחלט, מחלות תורשתיות אינן שכיחות, אולם המחלות התורשתיות המפורטות כאן מופיעות לעיתים קרובות בהשוואה למחלות אחרות הגורמות הגנטיות.
-
תסמונת מרפן
-
אנמיה בתאים מגליים
-
המופיליה (המופיליה A או B)
-
מוטציה של גורם V Leiden והתנגדות APC שהתקבלה
-
חולשה ירוקה אדומה
-
מחסור בגלוקוזה -6 פוספט דהידרוגנאז (מחסור ב- G6PD)
-
Polydactyly ("אצבעות מרובות", אפשרי גם כתסמין במחלות אחרות)
-
טריזומיה 21 (תסמונת דאון)
-
צ'ורטה צ'ינגטון
סיבות
מחלות תורשתיות מגוונות ביותר במראה שלהן. למעשה יש להם רק דבר אחד משותף: הסיבה לכל אחד מהם נעוצה ב- DNA, כלומר בחומר הגנטי של האדם הנוגע בדבר. שינויים שונים יכולים להתרחש כאן, כמו מוטציות (חילופי מידע ב- DNA) או מחיקות (היעדר חומר גנטי מסוים).
כמות גדולה של מידע מקודדת בחומר הגנטי, כמו למשל "טביעות התוכנית" עבור רכיבים שונים החשובים לתפקוד תא הגוף. אלה יכולים להיות אנזימים, תעלות אלקטרוליטים או חומרים מסנג'ר, למשל. האלמנטים הקטנים ביותר נקראים אז בצורה לא נכונה או בכלל לא מה- DNA, שאז חסר במערכת המתוחכמת של הגוף. המידע הגנטי הלא נכון או החסר גורם אפוא לתקלות מסוימות בגוף. לאחר מכן אלה גורמים לתסמינים לפי המערכת הפונקציונאלית בה חסר כעת מרכיב אחד.
גלה את כל הנושא כאן: הבדיקה הגנטית.
כך עוברים בתורשה מחלות תורשתיות
כל מחלה תורשתית עוברת בירושה מונוגנית או פוליגנטית: פירוש הדבר שישנו מיקום גנטי אחד או יותר שיש לשנות כדי להביא למחלה.
יתרה מזאת, תכונות גנטיות תמיד יכולות לעבור בתורשה באופן דומיננטי או רצסיבי: רצסיבי פירושו שיש להקדים את הגנים האבהיים וגם את הגנים האימהיים למחלה תורשתית מסוימת זו. במקרה של ירושה דומיננטית, די בשינוי אחד (כלומר הורה אחד) בכדי לעורר את המחלה. מכאן עולה כי עם מחלות שעברו בירושה באופן דומיננטי, האנשים הנשאים יחלו גם הם - ואילו עם ירושה רצסיבית לרוב כלל לא ידוע שיש נטייה גנטית מקבילה.
ישנן גם מחלות שעוברות בירושה דרך כרומוזומי המין, כמו המופיליה או עיוורון אדום-ירוק. המתקנים לכך הם בדרך כלל על כרומוזום X, מכיוון שכרומוזום Y הוא קטן מאוד בסך הכל ובאופן כללי יכול לאחסן מידע גנטי מועט. לפיכך מדברים על מחלות תורשתיות הקשורות ל- X. אלה בדרך כלל משפיעים באופן משמעותי על יותר גברים מאשר נשים, מכיוון שנשים יכולות לפצות על כל מידע שגוי בכרומוזום ה- X עם השני.
כיצד בדרך כלל עוברת בירושה של מחלה גנטית, בדרך כלל קל לחקור אם אתה מעוניין.
בדיקות לפני הלידה
באופן עקרוני, ניתן כבר לבדוק ברחם את החומר הגנטי של הילד בכל המחלות התורשתיות שמיקומן הגנטי הסיבתי ידוע. עם זאת, ניתוחים גנטיים גוזלים זמן, ולכן בדרך כלל מנותחים רק את מיקום הגן החשוד - לשם כך, בתורו, צריך להיות חשד מוצדק למחלה גנטית.
לבדיקה כזו ניתן לקחת חומר גנטי ממי השפיר או מהשלייה ולהשתמש בהם לניתוח.
עם זאת, יש לזכור תמיד כי כל אבחנה פולשנית כרוכה גם בסיכון לחיי הילד שטרם נולד. לפיכך יש לשקול נקבים כאלה בנפרד בכל מקרה.
ישנן מדידות שיכולות להצביע על מחלה גנטית, כמו מדידת השקיפות העורפית כסימן לטריסומיה 21. שיטות כאלה אינן מסוכנות עבור הילד שטרם נולד, אך אינן יכולות לספק וודאות מוחלטת בנוגע לנוכחותה של מחלה גנטית. אז גם כאן יש לקחת בחשבון פעולה כזו או אחרת.
טריזומיה 21
הגורם לטריזומיה 21 הוא כרומוזום 21, שאינו קיים פעמיים אלא שלוש פעמים אצל אנשים שנפגעו. וריאנט זה של ה- DNA נוצר כאשר הכרומוזומים מופצים בתאי הנבט ההורים, כלומר בתאי הזרע או ביצה. לפיכך מדובר ב"שגיאת התפלגות "ולא בשינוי בחומר הגנטי בפועל. זה מסביר מדוע טריזומיה 21 יכולה להופיע באופן ספונטני בכל משפחה ומדוע ההסתברות ללדת ילד עם תסמונת דאון זהה בכל המשפחות. באופן קפדני, אסור לספור את טריזומיה 21 - כמו טריזומיות אחרות כמחלה תורשתית במובן האמיתי. עם זאת, טריזומיה 21 היא המחלה הנפוצה ביותר ב- DNA בקרב ילודים.
תכונות של מערכת הכרומוזומים שהשתנו בתסמונת דאון כבר ניתן לראות אצל הילד שטרם נולד ברחם: עיכובים וגדלים בגדילה יכולים להוביל, בין היתר, לגולגולת קטנה מדי, עצמות קצרות בירך ובזרוע עליונה וליקויי לב. כמות גדולה של מי שפיר יכולה להיות גם אינדיקציה לטריזומיה 21, מכיוון שילדים שטרם נולדו מושפעים שותים או בולעים מעט יחסית מי שפיר. עם זאת, אף אחת מהתכונות הללו אינן סימנים מוחלטים לתסמונת דאון!
בנוסף לסימני פיגור הצמיחה שהוזכרו, ילדים עם תסמונת דאון לעתים קרובות מראים התפתחות עוכבת, למשל בתחומי השפה והמיומנויות המוטוריות. אנשים שנפגעים מתסמונת דאון מראים לרוב כישורים חברתיים ראויים לציון, ואילו אינטליגנציה לעיתים קרובות נותרה מתחת לממוצע. עם זאת, אנשים מושפעים זה מזה מאוד במאפיינים אלה, ולא נדיר שהם יסיימו את לימודיהם מבית הספר לאחר קבלת תמיכה טובה.
בהמשך החיים, אנשים עם טריזומיה 21 יש סיכון מוגבר לאבחון כחולים במחלות מסוימות. אלה כוללים מחלת אלצהיימר, אפילפסיה וסרטן, בעיקר לוקמיה. עם זאת, תוחלת החיים של אנשים עם תסמונת דאון ממשיכה לעלות: בינתיים אנשים מושפעים מגיעים לעיתים לגיל 60 או 70.
תוכל למצוא מידע נוסף באתר שלנו תסמונת דאון
מחסור באנטיטרפסין באלפא 1
מחסור באנטי-ריפסין באלפא 1 יכול ללבוש צורות וצורות שונות, תלוי במאפיינים הגנטיים המדויקים של האדם שנפגע. המשמעות היא שלא כל מחסור באנטה-1 של אלפא -1 מוביל לתסמינים. להלן, נדון רק בסוג הקליני הבולט (PiZZ) של מחלה זו שנקבעה גנטית.
מום האנזים הקיים במחלה זו גורם לפירוק ושיקום של אבני בניין ברקמת האיבר אצל אנשים מושפעים. בנוסף, החלבונים הפגומים מסוננים מהדם על ידי הכבד ומצטברים שם. זה יכול להוביל לדלקת בכבד (דלקת כבד), שחמת או סרטן הכבד. דרכי הנשימה שבריאות הופכות לא יציבות בגלל המחסור ברקמות יציבות והן קורסות יותר מהר: התמונה הקלינית של COPD (מחלת ריאות חסימתית כרונית) מתפתחת. תמונה קלינית זו היא לרוב הסימפטום הראשון של מחסור באנטה -1 של אלפא-1, ולכן יש לבדוק כל אדם הסובל מ- COPD בגיל צעיר יותר אם הוא חסר אנטי-טריפסין.
אם המחלה נמשכה זמן רב, הריאות עלולות להתנפח יתר על המידה, מכיוון שלא ניתן לנשוף את האוויר שאתה נושם כראוי דרך דרכי הנשימה הלא יציבות ולהצטבר לריאות. כטיפול, בנוסף להימנעות בעקביות מעישון סיגריות וחיסונים קבועים למניעת מחלות נשימה, יש לנקוט גם אמצעים רפואיים: ניתן לתת את אלפא-1-אנטיטריפסין החסר תוך ורידי בכדי להקל על הסימפטומים ככל האפשר ולהפסיק את מהלך המחלה.
תוכל למצוא מידע נוסף באתר שלנו מחסור באנטיטרפסין באלפא 1
דַמֶמֶת
קבוצת ההמופיליה ידועה גם בשם "המופיליה", שכן מונח זה מתאר את הסימפטום העיקרי של מחלה תורשתית זו באופן מדויק מאוד: האנשים שנפגעו מדממים זמן רב יותר, ובהתאם לחומרת המחלה, לעתים קרובות יותר מאשר לא הושפעו.
דימום נעצר בדרך כלל על ידי מה שמכונה מפל הקרישה, מסלול איתות אנדוגני המונע אובדן דם מופרז. במערכת קרישה זו 13 גורמים ממלאים תפקיד שמפעילים אחד את השני זה אחר זה. אפשר לדמיין את זה כסדרת דומינו: אם אתה מכה באבן אחת (גורם קרישה) זה מפעיל את הבא, וכן הלאה. בסוף מסלול האות הזה או הדומינו יש קרישת דם. בהמופיליה חסר גורם מסוים - תלוי בסוג הסוג הספציפי של המחלה: תגובת השרשרת מתנתקת כאן.
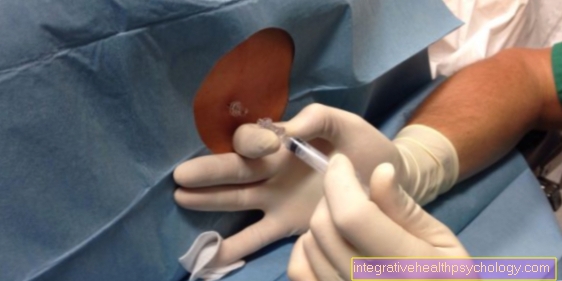
ניתן לבצע טיפול במחלה על ידי קביעת הגורם החסר והוספתו מבחוץ. לפיכך, אנשים מושפעים חייבים להזריק לעצמם באופן קבוע תכשיר עם גורם קרישה זה כדי ששאר תגובת השרשרת יכולה להתרחש.
תוכל למצוא מידע נוסף באתר שלנו מחלת דם
סיסטיק פיברוזיס
במחלה הגנטית סיסטיק פיברוזיס - המכונה גם סיסטיק פיברוזיס - קיימת ייצור לקוי של תעלות יון, ליתר דיוק של תעלות כלוריד. כתוצאה מכך, משתנה הרכב ההפרשות בגוף (למשל זיעה, הפרשות מדרכי הנשימה והלבלב) של האנשים שנפגעו: מכיוון שמחסור בכלוריד פירושו שפחות מים נמשכים לצינור הבלוטה המתאימה, ההפרשה צמיגה יחסית.
כתוצאה מכך, בדרך כלל מתפתחים תסמינים בדרכי העיכול, מכיוון שההפרשה עם אנזימי העיכול לא יכולה לזרום היטב מהלבלב למעי ובכך פוגעת בלבלב עצמו. בנוסף, נפוצות הפרעות עיכול כמו צואה שומנית, שלשול ומשקל הגוף הנמוך שנוצר.
הקבוצה הגדולה השנייה של התסמינים מתפתחת בדרך כלל בריאות: מכיוון שהריר המופיע באופן טבעי בריאות הוא צמיגי יותר מאשר אצל אנשים בריאים, קשה יותר להסיר אותו מהקליפה. זה יכול להוביל לשיעול כרוני וחסימת הסמפונות (הסמפונות). הכמות הגדולה יותר של הפרשת ריאות מספקת גם סביבה טובה לגידול חיידקים, מה שמביא לדלקות נשימתיות תכופות ודלקת ריאות.
טיפול בסיסטיק פיברוזיס מטופל באופן סימפטומטי באמצעות expectorants, אנזימי עיכול ואנטיביוטיקה לזיהומים.
תוכלו למצוא עוד על כך באתר האינטרנט שלנו סיסטיק פיברוזיס
גורם V Leiden והתנגדות APC
מוטציה של גורם V Leiden כוללת שינוי במידע הגנטי שיכול לגרום לקרישת דם מוגברת. הסיבה לכך היא גורם V במערכת מפל קרישת הגוף שנקרא: נתיב איתות זה מבטיח שבמקרה של פציעה, הפצע נסגר על ידי "חלבוני הדבקה" של הגוף (פיברין) עצמו. ישנם 13 גורמים בנתיב איתות זה, הנקראים בספרות רומיות (פירושו "גורם 5 סובל"!). לגורם V השפעה חיובית על היווצרות תקע פיברין, אך ניתן גם לעכב אותו מה שנקרא חלבון C מופעל (APC לזמן קצר). זה ממלא תפקיד חשוב בוויסות מסלול איתות זה ובמניעת קרישת דם מוגזמת.
הגורם המוטציה V קיים אצל האנשים הנגועים אך אינו מגיב ל- APC. בשלב זה חסר לגוף "אמצעי בטיחות" חשוב למניעת קרישת דם ללא סיבה, אשר עשוי אף לחסום את כלי הדם ובכך לגרום להפרעות במחזור הדם.
מבחינה סטטיסטית, אנשים שנפגעים ממוטציה V Leiden הם בעלי סיכוי גבוה יותר לחוות אירוע טרומבוטי (כלומר פקקת או תסחיף ריאתי), גם ללא היסטוריה של גורמי סיכון טיפוסיים. במונחים טכניים מדברים גם על "טרומבופיליה", כלומר נטייה להיווצרות קריש.
תוכלו למצוא עוד על כך באתר האינטרנט שלנו פקטור V ליידן
מחלת גושה
במחלת גושה, השינוי במידע ה- DNA גורם לפגם באנזים המעורב במטבוליזם של השומנים, ליתר דיוק גלוקוזרברוסידאז: הדבר מסייע בפירוק רכיבי תאים ישנים. במקרה של פגם, יכולה להיות ירידה בפונקציונליות או אפילו אובדן פונקציונליות, ובהתאם לכך הסימפטומים מופיעים בילדותם או בבגרותם הצעירה.
הסימפטומים של מחלת גושה נובעים במידה רבה מהגדלה של הכבד והטחול, שצמיחתם מנסה הגוף לפצות על מחסור באנזימים. זה מגביר את פירוק כל רכיבי הדם, אותם ניתן להכיר בספירת הדם ומשמש כמדד אבחוני יחד עם הכבד והטחול המוגדל.
האנזים הגלוקוצירברוזידאז החסר יכול לשמש טיפול תרופתי. הפרוגנוזה והמהלך של מחלת גושה תלויות במידה רבה בחומרת אובדן התפקוד של האנזים.
למידע נוסף, המשך לקרוא כאן: מחלת גושה.
מחלת אוסלר
מחלת אוסלר היא מחלה תורשתית המאופיינת על ידי התרחבות הדם החזקה. באופן עקרוני הרחבה זו של הכלים יכולה להתרחש בכל מקום, הן על העור והן על האיברים הפנימיים. קירות הכלים המוגדלים דקים יחסית וקרעים בקלות. כתוצאה מכך, האזורים הפגועים מדממים במהירות.
התרחבות הדם מתרחשת לעיתים קרובות במיוחד על הפנים ובקרום הרירית של האף, כך שהאנשים שנפגעו מתלוננים בדרך כלל על דימומים מהאף ודימומים מעט כתמים על הפנים.
אם יש חשד למחלה של אוסלר, יש לבצע אבחנה מתאימה, מכיוון שההשתנות יכולה להתרחש גם באיברים חיוניים או באיברים עם אספקת דם טובה, כמו הריאות, המוח או הכבד, בהם דימום מכלי קרוע מסוכן.
תוכלו למצוא מידע נוסף בנושא זה באתר האינטרנט שלנו מחלת אוסלר
מחלת רקלינגהאוזן
נוירופיברומטוזיס סוג 1 - או מחלת רקלינגהאוזן - היא מחלה גנטית בה לעתים קרובות הנפגעים מפתחים גידולים בתאי כיסוי העצב. הגידולים המתפתחים יכולים להיות גם שפירים וגם ממאירים ולהופיע בגיל צעיר.
עם זאת, גידולים אופייניים הם נוירופיברומות שפירות: אלה מורכבים מתאים המעטים ומבודדים את העצב כמו כבל חשמלי, כמו גם את רקמת החיבור שמסביב. הם שפירים, כלומר גידולים שאינם מתפשטים וגדלים לאט.
עם זאת, ניתוח להסרת נוירופיברומות יכול להיות קשה, מכיוון שלעתים קרובות הם מחוברים היטב לעצב וצריך להסיר את העצב המקביל. עם זאת, זוהי אפשרות הטיפול היחידה בנוירו-פיברומה סימפטומטית, מכיוון שלא ניתן לבצע טיפול סיבתי במחלה תורשתית זו.
תוכלו למצוא מידע נוסף בנושא זה באתר האינטרנט שלנו Neurofibromatosis סוג 1
ניוון שרירים
המונח ניוון שרירים מתאר קבוצה של מחלות תורשתיות בהן לא ניתן או להרכיב נכון רכיבי שריר מסוימים על ידי תאי הגוף. כתוצאה מכך, האנשים הפגועים בדרך כלל מפתחים חולשת שרירים כבר בילדות ובגיל ההתבגרות, וזה יכול לגרום לאובדן מסת שריר, הגבלות תנועה ואפילו מוגבלות פיזית.
אם יש חשד לנוכחות של ניוון שרירים, ראשית יש לקבוע את ערכי הדם. אם הערכים תואמים את האבחנה החשודה, עדיין ניתן לבצע ביופסיה של שריר: נלקחת דגימת רקמה קטנה מהשריר, אשר נבדקת לאחר מכן במיקרוסקופית לגבי מומים תאיים. ניתן גם לבחון בדיקה גנטית בכדי לבחון את האבחנה, שכן בדרך כלל המיקומים הגנטיים המתאימים ידועים בסוגים שונים של ניוון שרירים והיה צורך לשנותם. לא ידוע טיפול סיבתי לניוון שרירים.
תוכלו למצוא מידע נוסף בנושא זה באתר האינטרנט שלנו ניוון שרירים
Xeroderma pigmentosum
Xeroderma pigmentosum היא מחלה תורשתית נדירה בה אנזימים מסוימים בעורו של האדם הפגוע אינם פועלים. אנזימים אלו דואגים בדרך כלל לתיקון ב- DNA שעלול להיפגע מאור השמש או מאור ה- UVB הכלול. נזק ה- UVB יכול לגרום לסרטן עור בקרב אנשים מושפעים כמו גם אצל כל האנשים האחרים, אך עם Xeroderma Pigmentosum התהליך מואץ בגלל היעדר מנגנוני תיקון. כתוצאה מכך, האנשים המושפעים מפתחים צורות חמורות של סרטן העור בילדות ובגיל ההתבגרות ולאחר חשיפה קצרה לאור השמש.
טרם אפשרי טיפול סיבתי. האנשים שנפגעו צריכים להימנע מאור שמש לכל החיים, וזו הסיבה שהכינוי "ילדי אור ירח" ביסס את עצמו עבור האנשים שנפגעו (לעיתים צעירים מאוד). בנוסף, אנשים אלו צריכים להיות תחת פיקוח של רופא עור לצורך בדיקת סקר סרטן עור רגיל על מנת להסיר סרטן עור חדש שפותח לאחרונה. אם מקפידים על צעדים אלה בקפדנות, תוחלת החיים של אדם הסובל מ- xeroderma pigmentosum זהה לזו של אדם שאינו מושפע.
תוכלו למצוא מידע נוסף על מחלה זו באתר שלנו Xeroderma pigmentosum
תסמונת לינץ '
תסמונת לינץ 'היא שינוי ב- DNA הגורם לאנזים פגום בתאי הגוף.אצל האנשים שנפגעו, לפיכך מנגנון מסוים פגום, שאמור אחרת להגן על התאים מפני התנוונות, כלומר צמיחה בלתי מבוקרת - לאנשים עם תסמונת לינץ ', אם כן, יש סיכון מוגבר מאוד להתפתחות סרטן.
סרטן המעי הגס מתרחש לעתים קרובות כאן מכיוון שהתאים בדרך כלל מתחלקים כאן בכל מקרה, ושגיאות בתכנות הצמיחה והמוות של תא מורגשות במהירות רבה יותר. אנשים מושפעים מפתחים לעתים קרובות גידול במעי הגס בגיל צעיר במיוחד, כלומר לפני גיל 50, המכונה אז HNPCC (סרטן המעי הגס התורשתי שאינו פוליפוזי). עם זאת, לא כל מי שיש לו איפור גנטי של תסמונת לינץ 'יפתח סרטן המעי הגס. מצד שני, איברים אחרים יכולים גם לפתח גידול, מכיוון שהנטיות הגנטיות העדיפות את התפתחות הגידול קיימות בכל תאי הגוף. לפיכך יש צורך בבדיקות סדירות ובדיקות מניעה עבור אלו הנגועים בתסמונת לינץ 'על מנת לטפל כראוי בגידולים המתפתחים בשלב מוקדם.
תוכלו למצוא מידע נוסף בנושא זה באתר האינטרנט שלנו תסמונת לינץ '